Menstruacción
El ciclo menstrual comprende desde el primer día de la menstruación hasta el inicio de la siguiente, con una duración aproximada de 28 días.
En este periodo, la secreción de hormonas genera variaciones en la conducta, apetito, peso, temperatura y composición corporal.
El ciclo reproductor femenino se compone de 4 fases:
menstrual, pre-ovulatoria, ovulación y post-ovulatoria.
Fase menstrual
Se presenta durante los primeros 5 días del ciclo.
Se caracteriza por el desprendimiento de la capa funcional del endometrio. Al no producirse la fecundación del ovocito secundario liberado, se origina un sangrado (el flujo menstrual) y se liberan líquido intersticial, moco y células epiteliales.
Fase folicular
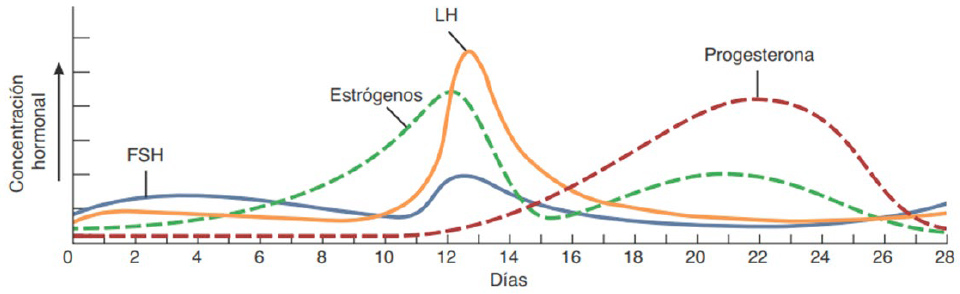
Comprende del día 1 al 13 e involucra el desprendimiento del endometrio (menstruación), durante esta fase, los estrógenos son las hormonas ováricas dominantes cuya secreción es estimulada por 2 hormonas adenohipofisarias: la hormona foliculoestimulante (FSH) y la hormona luteinizante(LH).
Se caracteriza por:
- Cambios en el sistema inmunitario: emociones +/-
- Mayor sensación de saciedad, disminución de la ingesta
- Mayor adhesión a un patrón alimentario saludable
- Metabolismo más elevado (aumento de la lipólisis)
- Más sensibilidad a la insulina, mayor tolerancia de los Hidratos de Carbono (HC)
Fase ovulación
Generalmente, tiene lugar el día 14 de un ciclo de 28 días y se caracteriza por la rotura de un folículo maduro, y la liberación de un ovocito, desencadenada por un pico de hormona luteinizante (LH).
Se caracteriza por:
- Menor tolerancia a los Hidratos de Carbono
- Mayor sensación de sed
Fase lútea
Comprende el tiempo que transcurre desde la ovulación hasta el inicio de una nueva menstruación. Se produce la formación del cuerpo lúteo en el ovario, con la secreción de grandes cantidades de progesterona y caída de los estrógenos.
Se caracteriza por:
- Menor serotonina a nivel del SNC
- Aumento del Gasto Metabólico Basal y apetito (¿GET?)
- Aumento de las necesidades energéticas
- Aumento de la temperatura basal: sudoración
- Menor sensibilidad a la insulina, poca tolerancia a los Hidratos de Carbono
Ciclo menstrual y emociones
Debido a los cambios hormonales producidos durante el ciclo menstrual, muchas mujeres padecen síntomas físicos y psicológicos. Estos síntomas suelen ocurrir durante la fase lútea, días previos a la menstruación, en la que los niveles de estrógenos están disminuidos y las concentraciones de progesterona son mayores.
También se producen cambios en la ingesta dietética y patrón alimentario, en función de las diferentes fases del ciclo menstrual.
Se ha reportado un incremento de la ingesta alimentaria y hambre emocional durante la fase lútea en comparación con la fase folicular y fase ovulatoria.
Food craving
Un deseo irresistible de consumir comida hiperpalatable.
Varía entre las diversas fases del periodo menstrual, dándose en mayor proporción durante la fase lútea y se ve incrementado días previos a la menstruación. A la progesterona, se le ha asociado un efecto orexígeno
(mayor apetito). En cambio, los estrógenos, se asocian a un efecto anorexígeno (menor apetito).
No se ha observado que en todas las mujeres exista un mayor deseo por los alimentos hiperpalatables más alla de la que se pueda tener normalmente, por lo que no hay que usar la menstruación como excusa. Se necesita más homogeneidad y estudios experimentales que corroboren estos resultados.
Herramientas
- Respetar el ritmo circadiano.
- Aumentar el consumo de alimentos con gran densidad nutricional para aumentar la saciedad.
- Alimentación anti-inflamatoria: fitoquímicos, w-3 (atún, trucha, salmón, sardina, nueces, semillas de lino), baja carga glucémica, crononutrición…
- Vitaminas del complejo b (cereales integrales, legumbres, carne, pescado y lácteos): mantienen una estrecha relación con la serotonina (hormona de la felicidad), que ayuda a contrarrestar la irritabilidad y disminuye el dolor abdominal.
- Hierro: en casos de anemia causada por las hemorragias (origen animal, frutos secos, verduras de hoja verde y cítricos)
- Vitamina C: para aumentar la absorción del hierro y disminuir la migraña menstrual ( limones, limas, naranja, fresa, mandarina, kiwi…)
- Fibra: promueven la eliminación de estrógenos y alivian el dolor (Alcachofa, col, berza, ajo, frambuesa, granada, legumbres…)
- En mujeres que se observa food craving, el dolor, edema… podría provocarse por el tipo de alimentación (picoteos, atracones, hidratos de carbono refinados).
- Reducir las bebidas estimulantes: café, té… en caso de irritabilidad, nervios, exaltación…
- Ejercicio físico adaptado para disminuir la inflamación
- En la fase lútea debemos aumentar el consumo de agua para combatir la retención.
Referencia bibliográfica
- Moreno Gómez E, Jáuregui-Lobera I. Variables emocionales y food craving: Influencia del ciclo menstrual. JONNPR. 2022;7(1):28-63. DOI: 10.19230/jonnpr.4429
- Aquino, Camey, M. (2015). Intervención nutricional para la disminución de síntomas del síndrome premenstrual. Estudio realizado en clínicas privadas de la ciudad de Guatemala. Licenciatura. Universidad Rafael Landívar.
- Marnet, M. (2013). “Ciclo menstrual”, en CCM Salud. . Navarro Castelló, I. (2015). Estudio sobre la influencia del ciclo menstrual en la conducta alimentaria. Licenciatura. Universidad de Lleida.
- Núñez, G. (2018). “Ciclo menstrual y nutrición”. . Ortega Ana, R. y Requejo Marcos, A. (2015). Nutriguía: Manual de nutrición clínica en atención primaria. Madrid: Editorial Complutense, pp.59-60.





